パーキンソン病の治療
監修:京都大学 総合研究推進本部 参与 特定教授 髙橋 良輔 先生
パーキンソン病の治療は薬物療法とリハビリテーションが中心となります。しかし、薬物療法をはじめて数年たつと、薬の効果が切れて動けなくなってしまったり、薬の作用が強く出て、体が勝手に動いてしまったりすることなどがあります。こうした症状で生活に支障がある場合などはデバイス補助療法やその他の治療が検討されます。ここでは、パーキンソン病の治療を「薬物療法」、「デバイス補助療法」、「その他の治療」に分けて解説します。リハビリテーションについては、以下リハビリテーションの重要性をご覧ください。
薬物療法
パーキンソン病の薬物療法の主軸となるのは、少なくなったドパミンを補う薬です。ドパミンそのものを補う薬や、ドパミンの減少をおさえる薬などがあります。
しかし、パーキンソン病治療薬を長期間にわたり使用していると、薬の効果が持続しなくなり、薬の効果が切れて体が動かなくなったり(ウェアリングオフ)、身体が
勝手に不自然に動いてしまったり(ジスキネジア)することがあります。
そこで、症状や副作用の程度に合わせて、複数の薬を組み合わせたり、服薬回数や服薬時間を調整しながら治療するのが一般的です。
薬によって、服薬のタイミングや特性が異なりますので、その理由をよく理解して服薬することが大切です。また、パーキンソン病の治療薬以外の薬を併用するときには、
飲み合わせに注意する必要があります。服薬するお薬の詳細は主治医や薬剤師に確認してください。
パーキンソン病の治療に使用される主な薬剤と作用
| 薬剤 | 作用 |
|---|---|
| レボドパ含有製剤※ |
薬物療法の中心となる薬です。脳内でドパミンに変化して、不足しているドパミンを補います。服用してから効果があらわれるまでの時間が短い(即効性がある)という特徴があります。
|
| ドパミン受容体刺激薬 | レボドパと同様、薬物療法の中心となる薬です。ドパミンに似た作用をもち、脳内でドパミンを受け取るドパミン受容体に結合します。レボドパより持続時間が長いのが特徴です。 |
| MAO-B(マオビー)阻害薬 | ドパミンを分解するMAO-Bという酵素の働きをおさえ、ドパミンを脳内に長くとどまらせます。 |
| COMT(コムト)阻害薬 | 血液中のレボドパの分解をおさえ、脳に送り込まれるレボドパを増加させます。 |
| ドパミン放出促進薬 | 脳の神経細胞からドパミンの放出を促す作用があります。ジスキネジアをおさえる効果があります。 |
| 抗コリン薬 | 神経伝達物質であるドパミンとアセチルコリンのアンバランスがパーキンソン病の症状を引き起こしていると考えられており、抗コリン薬はアセチルコリンとドパミンのバランスを整えます。 |
| ノルアドレナリン補充薬 | ノルアドレナリンは、ドパミンと同じ神経伝達物質で、ノルアドレナリンに変化する薬を補充することによって、「すくみ足」、「起立性低血圧」の症状に効果があると考えられています。 |
| レボドパ賦活薬 | 体内でドパミンが作られるのを促進したり、ドパミンを分解する酵素の働きをおさえることにより、脳内のドパミンを増やします。 |
| アデノシン受容体拮抗薬 | アデノシン受容体は運動機能の調節に関係していると考えられており、アデノシン受容体拮抗薬は進行期の「オフ」の時間を短縮する効果があると考えられています。 |
- (参考)
- 病気がみえる vol.7 脳・神経 第2 版. メディックメディア, p352, 2018.
- 織茂智之監修:患者のための最新医学 パーキンソン病 改訂版. 高橋書店, p52, 2023.
薬の影響と注意点
ウェアリングオフ
パーキンソン病治療薬を長期間にわたり使用していると、薬の効果が持続しなくなり、薬の効果が切れて体が動かなくなってしまう症状が出ることがあります。薬が効いている状態(オン)と効果が切れた状態(オフ)があらわれる現象を「ウェアリングオフ」といいます。特にレボドパ服用時によく見られますが、他の薬でも起こることがあります。

ジスキネジア
パーキンソン病治療薬を長期間にわたり使用していると、体幹、手足、首、口などが自分の意志に関係なく動いてしまうことがあります。これを「ジスキ ネジア(不随意運動:ふずいいうんどう)」といいます。特にレボドパ服用時によく見られますが、他の薬でも起こることがあります。

これらのほかに、吐き気、むくみ、立ちくらみ、日中の強い眠気や突然の眠気発作、幻覚、ギャンブルや 買い物、過食などがやめられなくなる衝動制御障害などの症状があらわれることがあります。 症状の程度や起こりやすさは薬の種類や量によって異なりますので、気になる症状があれば 主治医や薬剤師に相談してください。


- (参考) 病気がみえる vol.7 脳・神経 第2 版. メディックメディア, p348, 2018.
デバイス補助療法
薬物療法で症状のコントロールが難しい場合や、副作用が強くあらわれたりする場合には、機器を使用する治療法(デバイス補助療法)を選択する場合もあります。
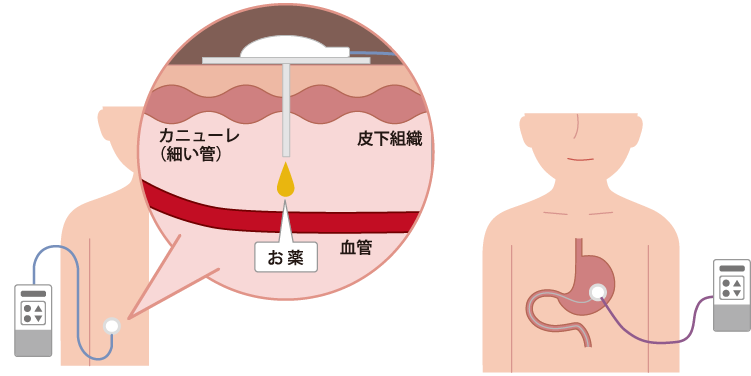
① 持続皮下注療法と経腸療法
持続皮下注療法とは、カニューレと呼ばれる細い管を皮膚に留置して、チューブを通じてポンプで24時間持続的に皮下に薬を投与する治療法です。経腸療法とは、胃ろうを造設し、カセットに入ったレボドパ製剤を、専用ポンプとチューブを使って薬剤の吸収部位である小腸に直接持続的に送り届ける治療法です。どちらの治療も機器を使って安定的にレボドパを体内に投与できるため、薬の効果が切れてしまったり、逆に効きすぎてしまう時間を減らすことが期待できます。
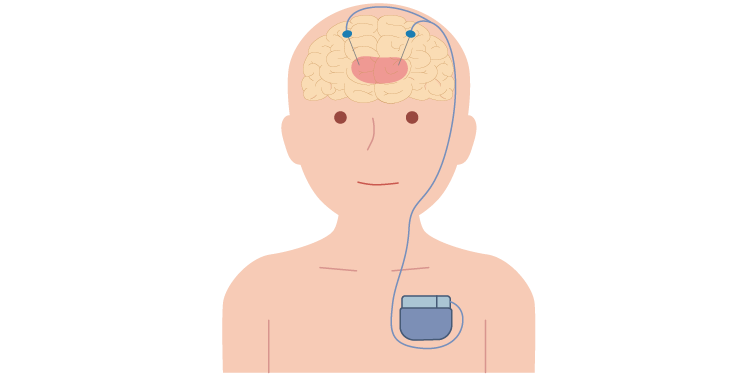
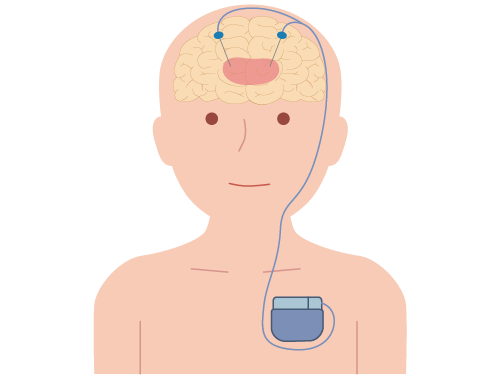
② 脳深部刺激療法(DBS)
脳の中に電極を入れ、体内に埋め込んだ刺激装置で電気刺激を与える治療法です。刺激することによって、神経の異常な働きがおさえられ、そこを凝固(破壊)したのと同じような効果が得られます。また、刺激の設定を適切に行うことによって、パーキンソン症状を細かくコントロールできます。そのため、手術後も定期的に刺激装置の調整が必要になり、一定期間で刺激装置の電池交換も必要になります。この治療は定位脳手術という方法で脳内に刺激装置が留置されます。定位脳手術とは、頭蓋骨に固定したフレームと脳内の目標点の位置関係をCTやMRI で確認し、外から見ることのできない脳内の目標点に正確に到達する技術です。頭蓋骨に開けた小さな穴から針を刺すだけなので、手術による負担は軽くて済みます。
その他の治療
薬物療法で症状のコントロールが難しい場合や、副作用が強くあらわれたりする場合には、その他の治療も選択肢になります。その他の治療には、脳の中で活動に異常をきたしている部分を熱凝固する治療(①凝固術)や、ドパミンを増やすために細胞を移植する治療(②細胞移植治療:日本で条件及び期限付で承認)があります。
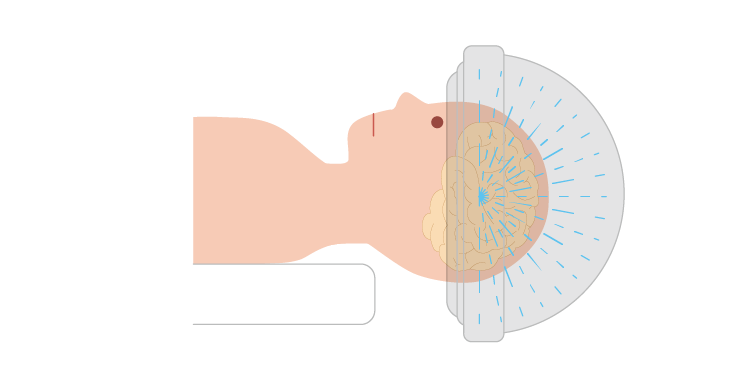
① 凝固術
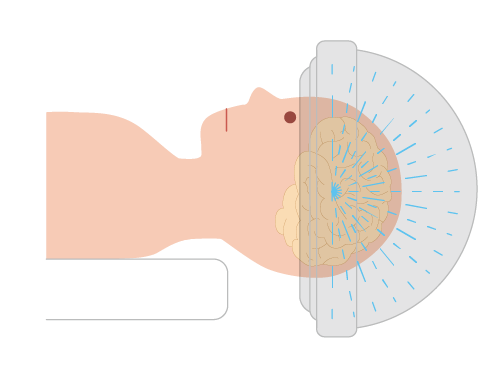
脳の中の淡蒼球や視床とよばれる部分がそのターゲットとなっており、MRIでこれらの部位を同定して、定位脳手術によって電極で部分的に熱凝固します。近年では治療用ヘルメットを装着し、MRIガイド下で超音波を用いて熱凝固する治療(MRgFUS)もあります。超音波を用いる方法では頭蓋骨に穴をあける手術が不要であることが特徴です。
② 細胞移植治療
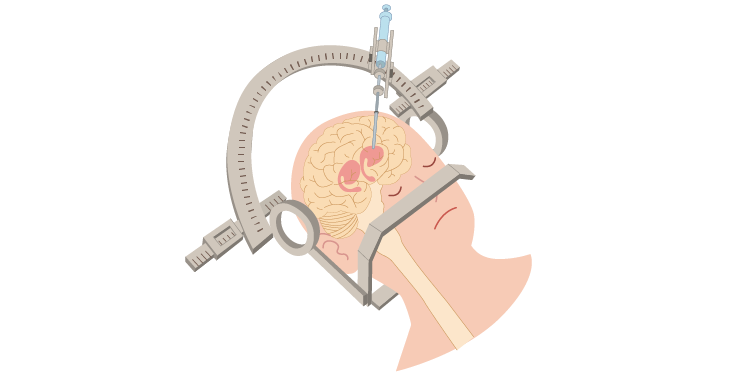
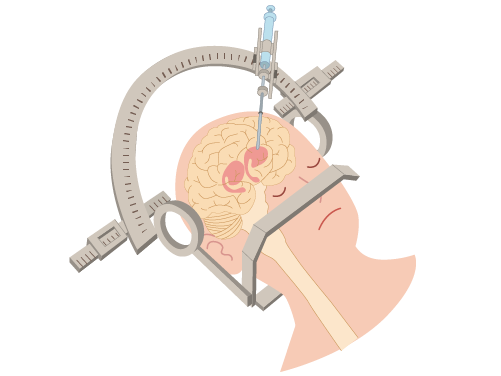
細胞移植治療とは、ドパミン神経のもととなる細胞を脳の中に移植する治療をいいます。失われたドパミン神経細胞を脳内に補充し、運動機能を改善させることを目的としています。ドパミン神経のもととなる細胞はiPS細胞の技術を用いて作成されています。手術では、頭蓋骨に小さな穴をあけ、専用の機器を使って定位脳手術で脳内に細胞を移植します。
- (参考)
- 下泰司:JOURNAL OF CLINICAL REHABILITATION 34(6): 580-585, 2025.
- 織茂智之監修:患者のための最新医学 パーキンソン病 改訂版. 高橋書店, p104, 2023.
- 前田哲也ほか著:みんなで学ぶパーキンソン病 患者さんとともに歩む診療をめざして. 改訂第2 版. 南江堂, p61, 2020.
- パーキンソン病療養の手引き https://plaza.umin.ac.jp/~neuro2/parkinson.pdf(2026 年1 月閲覧)
- 森実飛鳥:日本臨牀 81(8): 1259-1264, 2023.